一人ひとりに合った最適な心房細動治療を目指して。
心房細動を患う全ての患者さんに「遺伝的素因」に基づくあなただけの治療を。
FUTURE-AF Studyホームページをご覧いただきありがとうございます。佐賀大学循環器内科・先進不整脈治療学講座の山口尊則です。私たちは、心臓(脈)が速く打つ、ゆっくり打つ、または不規則に打つ状態である「不整脈」という心臓病に対する最先端の治療と研究を行っています。
不整脈の中でも脳梗塞・心不全の原因となる「心房細動」という不整脈の原因解明とそれに対する最適な治療法の確立はまだ不十分です。心房細動は数多くの遺伝的素因によってその性格(個性)が決まると予想されますが、心房細動の遺伝情報に関する研究はまだ十分に進んでいないのが現状です。
そこで、佐賀大学循環器内科に事務局を置く「 FUTURE-AF研究」が進行中です。この研究は5,000人という世界的にも最大規模の患者さんにご参加いただき、個々の患者さんの遺伝情報と心房細動治療の予後の関係を観察する研究です。そして、将来的には(in the FUTURE)、心房細動を患う全ての患者さんに、一人ひとりに合った最適な「あなただけの」心房細動治療(=遺伝情報に基づく個別化医療)を提供することを最終目標としています。
本ページでは、心房細動という病気、心房細動によって引き起こされる合併症、心房細動に対するカテーテルアブレーション、心房細動の原因、心房筋の変性、そして遺伝的要因との関係などについて解説しております。

脳梗塞・心不全の原因となる「心房細動」とは?
心房細動(しんぼうさいどう)とは?
心臓(脈)が速く打つ、ゆっくり打つ、または不規則に打つなど心臓のリズムが乱れる病気の総称を「不整脈」といいます。
その不整脈の中でも最も頻度が高く、適切な治療が必要な病気が「心房細動」です。心臓は左右の心房と左右の心室の4つの部屋から構成されます。このうち左右の心房が小刻みに痙攣し、脈が早くなったり遅くなったり不規則なリズムになる状態が「心房細動」です。
この「心房細動」の怖いところは、脳梗塞・心不全など命に関わる病気の原因となるところです。心房が細かく震え、心房の中で血液の流れがよどむことにより、「血液の固まり(血栓)」ができ、それが血流に乗って全身に運ばれ、脳の血管を詰まらせると脳梗塞に至ります。脳梗塞になれば、手足の麻痺や寝たきりになってしまうこともあります。

また、心房細動中は心房が有効に収縮しないため、心房から心室へ十分に血液が送れなくなったり、心房細動に伴う早い脈拍が続くことで心室のポンプ機能が低下したりすることにより、心不全に至ることもしばしばあります。心不全を発症すると息切れやむくみなどの症状が重篤となり、入院治療や追加の薬物治療が必要になります。
「心房細動」を発症すると、動悸や胸が苦しい、息切れがしやすい、疲れやすいなどの自覚症状が出ますが、「年をとったから」と思われている方の中に、その原因が心房細動であることもよくあります。一方、全く無症状の方もおり、脳梗塞や心不全を発症してから心房細動と診断されることもあります。
日本で心房細動を患う患者さんは2005年の時点で70万人以上、2050年には100万人を超え、総人口の約1%を占めると予測されています*1が、心房細動の持続時間が短い方や無症状の方は心房細動の正確な診断が難しいことも多く、実際の患者数はこの予測の2倍以上いるのではないかと私たちは考えています。
心房細動の治療方法とその課題
心房細動の治療方法は?
心房細動の治療は、薬物療法による自覚症状のコントロール、脳梗塞の予防、心不全の予防があります。しかし、薬物療法では心房細動そのものを消失させることはできません。
そのため、心房細動そのものを消失させる、または自覚症状や頻度を減らす治療法として、カテーテルアブレーションという手術法が開発されました。
心房細動は、心臓の一部(主に4本の肺静脈)から発生する異常な電気信号がきっかけとなって起こることが多いため、その発生起源に対して、カテーテルという細い管を用いて焼灼や冷凍凝固を行う治療法です。
日本では、2019年には年間6万件の心房細動に対するカテーテルアブレーションが行われました*2。
佐賀大学でのカテーテルアブレーション中の様子は下記リンクよりご覧になれます
この治療を受けた患者さんのおよそ80-90%は心房細動が消失し、正常の脈が維持できます。しかしながら、10-20%の患者さんは、アブレーション後も心房細動が再発してしまいます。またアブレーション後の再発に対して、補助的な薬物療法が有効な方もいますが、その効果が低い方もいます。また長年の経過で、術後に消失していた心房細動が再び出現することもあります。
同じ心房細動でありながら、薬による治療やカテーテルアブレーション後の経過が異なることは、この治療に携わる我々医師や研究者にとっては全力で解決すべき大きな課題です。
心房細動が再発してしまう理由の1つに「心房筋の変性」があります。
心房筋の変性を直接調べるための検査は、その危険性から研究が進んでいませんでした。
カテーテルアブレーション手術を受けた方のうち、10-20%の患者さんに心房細動が再発してしまう理由は、①カテーテルアブレーション時に見つけることができなかった起源から心房細動が出現すること、②心房筋が変性することで心房細動の起源が次々と出現すること、③心房筋の変性により心房細動が容易に持続してしまうことです。
①の原因であれば、複数回のアブレーション治療によって心房細動を消失させるチャンスは高くなりますが、②③のように心房筋の変性がいったん進行すると現行の薬物療法やアブレーション治療では、心房細動を長期的に消失させることは難しくなります*3-7。
さまざまな生活習慣病や加齢の影響、その他明らかになっていない原因により、心房筋の変性が出現します。決して悪性ではないのですが、いわゆる「がん」のように心房筋の変性は少しずつ進行していきます。
この心房筋の変性は「線維化」というプロセスが主体と考えられてきました3-7。線維化とは「細胞と細胞の間に結合組織と呼ばれる部分が異常に増殖し、その結果臓器が障害される」ことです。
心筋の変性を診断するには、心筋を1~2ミリほど採取して顕微鏡で確認する方法がとられます。これを「心筋生検による組織学的評価」といい、従来は心臓の壁の厚い心室筋のみが心筋生検の対象でした。
一方で、心房の壁の厚さは5ミリ前後で非常に薄く、そこから1~2ミリの心筋を採取してしまうと、場合によっては心房壁に穴を開けてしまう危険があるため、心房筋から心筋生検を行うことは困難と考えられてきました。このため、実際には心房筋変性の研究は進んでいませんでした。
安全な「心房生検」の検査方法を開発!
遺伝的要因が心房の変性や心房細動の発症・再発に大きな影響を与えている可能性が。
私たちは心房細動治療の発展には、心房筋の変性を直接診断することが必要であると考えてきました。そこで私たちは、心房細動患者さんにおける安全な心房筋生検の方法を開発しました。それが、心房内からカテーテル型の超音波装置を用いて、心房の中央部分から心房筋を安全に採取する方法です。この研究結果は2022年3月に『Journal of the American Heart Association誌』にオンラインで掲載されています*8。
https://www.ahajournals.org/doi/10.1161/JAHA.121.024521
これまで研究にご協力いただいた300例以上の患者さんから心房生検を行いましたが、検査は短時間で終了し、安全性も全く問題ないことがわかっています*9。
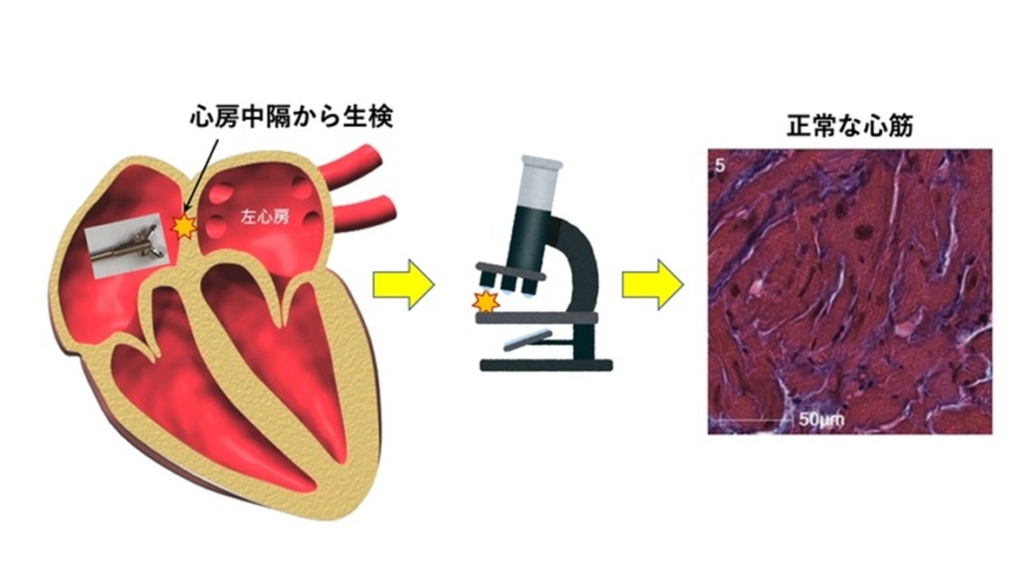
この手法による心房筋生検により、ようやく心房筋変性の顕微鏡による組織学的な評価が可能になりました。また、驚くことに、心房筋の変性は線維化だけでなく、その他さまざまなタイプの変性があることが判明しました。
さらに驚くべきことに、生活習慣病のない比較的若い患者さんでも心房筋の変性が進んでいることもあれば、多数の生活習慣病があったり、ご高齢であっても心房筋の変性が少ない患者さんもいることがわかりました。
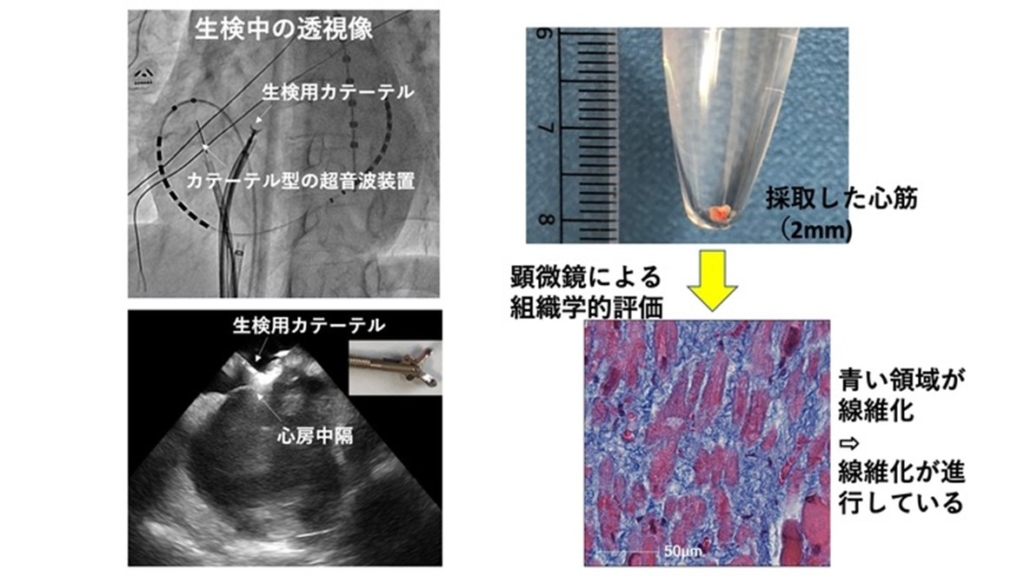
この心房生検の結果に基づき、どのような変性がどの程度あればアブレーション後に心房細動が再発してしまうのか、を調査するために、現在、佐賀大学および大分大学にて350人規模の観察研究が進行しており、3年後には研究結果が判明する予定です(HEAL-AF, HEAL-AF 2 study)*10。
研究を進めるうちに、生活習慣病や加齢だけでなく、やはり遺伝的要因(遺伝的多型)が心房の変性や心房細動の発症・再発に大きな影響を与えているだろうという仮説が生まれました。
私たちの遺伝情報はDNAによって担われています。DNAの塩基配列の99.9%は万人に共通ですが、残りの0.1%は個人によって異なります(遺伝的多型)。そしてこの違い=遺伝的多型は両親から受け継いでいます。またこの違いこそが、個人が有する遺伝的な個性=性格=体質になります。例として、血液型、お酒の強さ、太りやすさもこの違いによって説明されます。
遺伝的多型は少なくとも100人中1人以上の人が持っている遺伝情報の違いのことで、1つの遺伝的多型だけで直接病気が引き起こされるほど強い影響力があるものではありません。しかし、この違いが積み重なることによって、そして食事や生活習慣などの環境も重なることで、心房細動を含むさまざまな病気を発症しやすくなることがわかってきました*9。
個々の患者さんの心房細動の性格に応じた治療法の開発へ向けて
そこで私たちは2021年9月から、心房細動アブレーションを行う5,000人もの大規模の患者さん群において、極少量の血液をいただき、そこから得られた遺伝情報と治療後の経過がどのように関連するかを調べる「FUTURE-AF研究」を開始しました*11。
遺伝的素因に基づく心房細動アブレーション後の長期的予後と予測因子の評価
Follow-Up study of paTients UndeRgoing cathEter ablation for Atrial Fibrillation: evaluation of long-term outcomes and predictive factors based on genetic predisposition (FUTURE-AF Study)
この研究は日本各地の病院、理化学研究所、東京大学循環器内科など多くの施設と共同で研究を行っています(共同研究施設一覧参照)。
この研究が進むことで、将来的には採血によって得られた遺伝情報をもとに、個人個人の心房細動の性格に合った、オーダーメイドの心房細動治療(=個別化医療やゲノム医療)が提供できると考えています。
例えばある遺伝素因を持った患者さんには、通常のアブレーション治療(肺静脈隔離術)だけでなく、その方に合った追加のアブレーション方法を選択することができるでしょう。またアブレーション手術の合併症が生じやすい患者さんを事前に予想することで、合併症を避けるための治療方針を選択することも可能になるでしょう。また術後の再発リスクや脳梗塞・心不全の発症リスクが高いと予想される患者さんには、術後の薬物療法や生活習慣の管理を強化することで、これらのリスクを最小化することも可能になります。薬物治療による副作用のリスクに応じて個々の患者さんで最適な薬物が選択ですることも可能になるでしょう。
このようにして、一人ひとりの患者さんに合った最適な治療法を提供することで、心房細動治療の成功率を高め、脳梗塞・心不全を予防し、同時に合併症や副作用などのデメリットを最小化できると期待しています。またこのような個別化医療は医療費の削減にもつながることも期待できます。
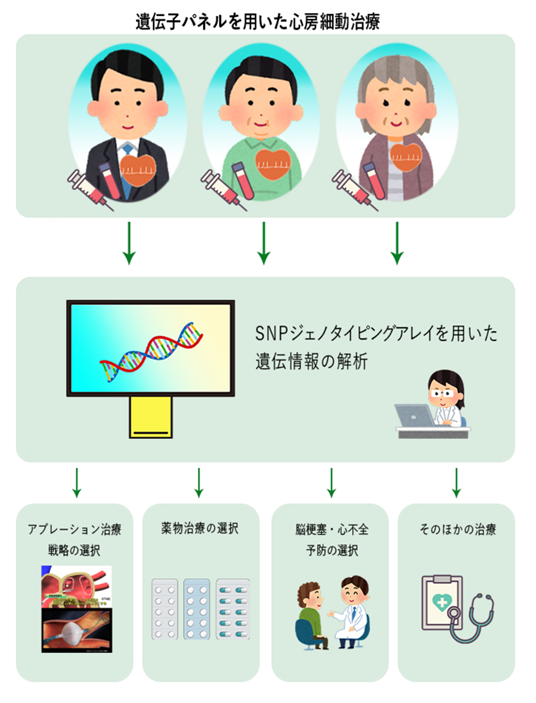
この心房細動という複雑な不整脈に対して、患者さん一人一人の心房細動の性格を見抜くことで、それぞれの患者さんに最適な治療法を提供し、治療全体の成功率を高めたい。我々はそのような強い思いで研究を続けています。
個別化医療の実現が、私たちが医師・研究者人生をかけて到達するべき最終目標の1つだと思っています。世界中の心房細動患者さんの未来のために、日本全国の病院や研究施設のみなさまとともにこの研究を進めて参ります。
参考文献
*1: Inoue H, et al. International Journal of Cardiology 2009:137;102–107
*2: Kusano K, et al. J Arrhythm. 2021;37:1443-1447.
*3: Yamauchi T et al. Europace. 2014;16:511-20.
*4: Marrouche NF et al. JAMA. 2014;311:498-506.
*5: Yamaguchi T, et al. J Cardiovasc Electrophysiol. 2016;27:1055-63.
*6: Yamaguchi T, et al. J Cardiol. 2018;72:427-433.
*7: Takahashi Y, Yamaguchi T, et al. Circ J. 2020;84:1254-1260.
*8: Yamaguchi T, et al. J Am Heart Assoc. 2022;11:e024521.
*9: Otsubo T, Yamaguchi T, et al. 論文投稿中および2021年日本循環器学会学術集会発表
*10: UMIN臨床試験登録システム UMIN000040781及びUMIN000044943
*11: UMIN臨床試験登録システム UMIN000046658
